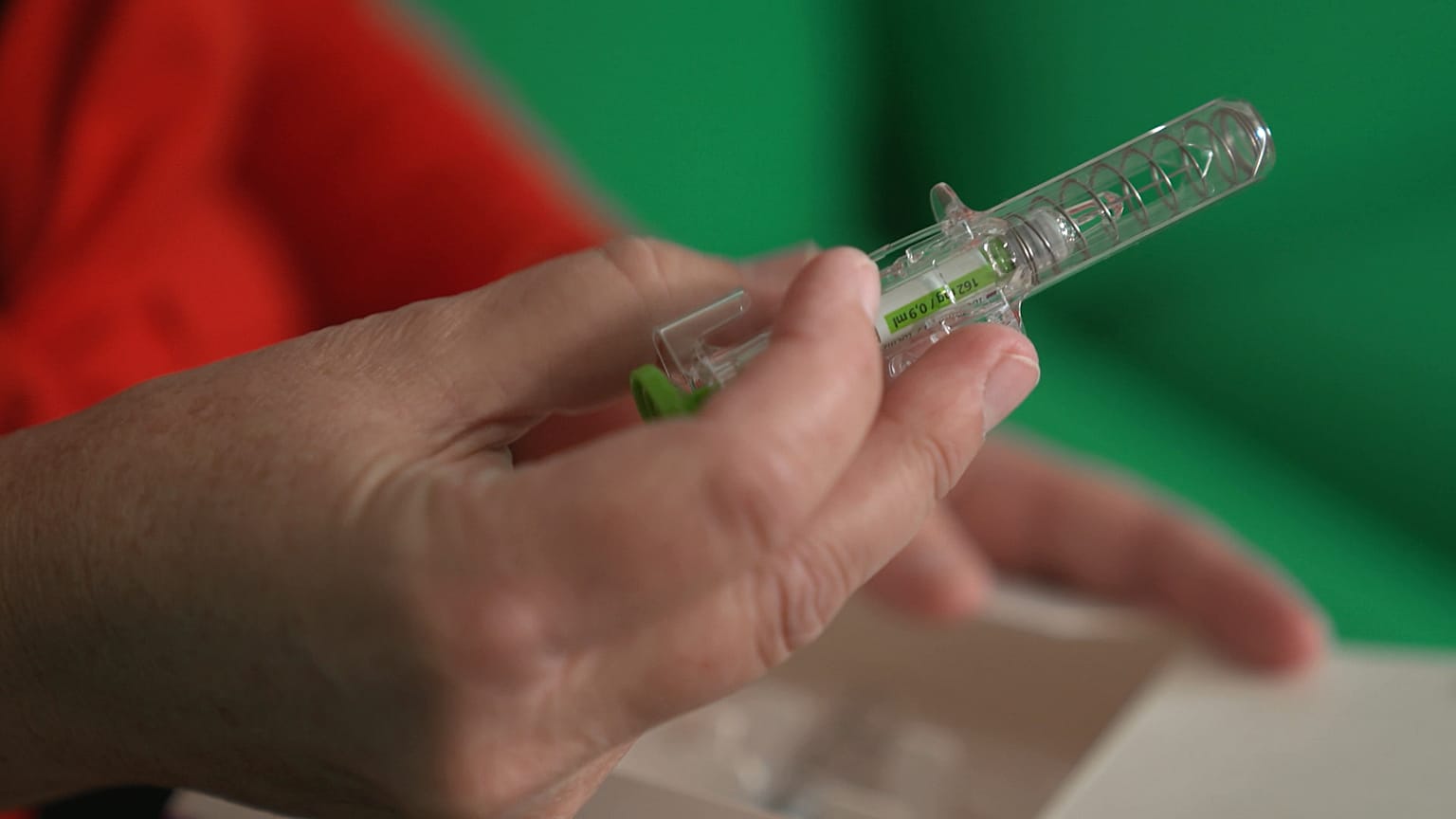
Im Rahmen ihrer Reform des Arzneimittelrechts will die EU die Verwendung von Biosimilars fördern, d. h. von Produkten, die weniger kosten und genauso wirksam sind wie die Originalmedikamente. Wir sehen uns das in Dänemark an, das eine Vorreiterrolle in diesem Bereich einnimmt.
Connie Ziegler kann sich nicht mehr daran erinnern, wann ihre gesundheitlichen Problem angefangen haben. Ihre Eltern sagten ihr, sie war etwa anderthalb, als ihre Knie wehtaten und sie nicht mehr weit gehen wollte. Die Schmerzen fingen an. Kurz darauf, nach den ersten Symptomen, wurde bei ihr eine juvenile rheumatoide Arthritis diagnostiziert.
 WERBUNG
WERBUNG
 WERBUNG
WERBUNG
Heute mit 54 Jahren arbeitet Connie als Projektmanagerin bei der Dänischen Rheumavereinigung Gigtforeningen in Kopenhagen.
Ihre Behandlung begann mit Anfang 20. Vor etwa zehn Jahren rieten ihr die Ärzte, ihre normale Medikation durch Biosimilars zu ersetzen.
Biosimilars sind biologische Arzneimittel, deren Struktur, Wirksamkeit, Sicherheit, Dosierung und Nebenwirkungen denen der zugelassenen Referenzarzneimittel sehr ähnlich sind. Sie sind jedoch billiger in der Herstellung und für Patient:innen und Gesundheitssysteme erschwinglicher.
Dänemark ist Vorreiter bei den Biosimilars
"In manchen Phasen meines Lebens hat es eine ganze Weile gedauert, bis ich die richtigen und guten Medikamente gefunden habe. Deshalb war ich besorgt, als mir gesagt wurde, dass ich auf ein Biosimilar umgestellt werden sollte: Würde es genauso gut wirken?", beschreibt Connie Ziegler ihre anfänglichen Bedenken.
"Aber ich dachte auch, dass sie es mir nicht geben würden, wenn es nicht in Ordnung wäre. Ich war also bereit, es zu versuchen. Es gab eine andere Packung, die sah ein bisschen anders aus. Aber bei mir hat sich nichts geändert, weder in der Behandlung noch in meinen Empfindungen.”
Wie Connie haben Tausende dänische Patienten in den letzten Jahren erfolgreich auf Biosimilars umgestellt. Dänemark ist ein Vorreiter bei der Verwendung von Biosimilars. Das Land hat auch eine gute Tradition bei der Überwachung seiner Patient:innen.
Sobald Biosimilars verfügbar waren, haben Experten angefangen, ihre Auswirkungen zu untersuchen. Bente Glintborg war an einer Reihe dieser Studien beteiligt.
"Als die Biosimilars auf den Markt kamen, lag es für uns auf der Hand, diese Daten prospektiv zu betrachten: das heißt, die Patienten, die auf ein anderes Medikament umgestellt wurden: Wie verhalten sich die Ergebnisse der Patienten, wie ist die Wirksamkeit des Medikaments, ist sie gleich?", so die Beraterin am Zentrum für Rheumatologie Glostrup.
Wirkung und Qualität sind absolut identisch
In einer Vergleichstudie mit mehr als 1.000 Patienten waren die Ergebnisse fast identisch. "Wir konnten die Linien kaum auseinanderhalten. Das hat uns gezeigt, dass die Patienten die Umstellung auf die Biosimilars annehmen und die gleichen Ergebnisse erzielt werden, wie mit dem Originalpräparat."
Im Lichte dieser Durchbrüche will die Europäische Kommission mit ihrer Pharmareform die Verfügbarkeit von Biosimilars - und auch von Generika - verbessern, damit mehr Patienten Zugang zu erschwinglicheren Medikamenten bekommen. Biosimilars sollen bis zu zwei Jahre früher als heute auf den Markt kommen.
Von den Niederlanden aus wird die Europäische Arzneimittel-Agentur weiterhin eine Schlüsselrolle auf der Ebene der Beratung und Regulierung spielen.
Das erste Biosimilar wurde von der Agentur bereits 2006 zugelassen. Seitdem wurden 105 Biosimilars in der Europäischen Union freigegeben. Die Kandidaten stehen unter strenger Beobachtung, erklärt Steffen Thirstrup, Chief Medical Officer bei der Arzneimittel-Agentur.
"Was wir hier suchen, ist die Gewissheit, dass der Hersteller diese Produkte auf konsistente und sichere Weise herstellen kann. Wir wollen sicher sein, dass er das herstellt, was er versprochen hat, und dass er nachgewiesen hat, dass das Produkt auf molekularer Basis dem Referenzprodukt ähnlich ist.
Einige Kritiker und diejenigen, die Zweifel an Biosimilars haben, würden argumentieren, dass die Standards niedriger sind. Aber das ist absolut nicht richtig. Wir würden unabhängig von der Art des Arzneimittels, mit dem wir es zu tun haben, die gleichen Standards anlegen. Als Generika vor 30 oder 40 Jahren eingeführt wurden, hatten wir die gleichen Bedenken. Es gibt immer noch ab und zu Gerüchte, dass Generika, weil sie billiger sind, eine geringere Qualität haben. Das ist aber nicht wahr.
"Die rheumatoide Arthritis ist eine chronische Krankheit, und es ist nicht nur wichtig, wie der Zustand heute ist, sondern auch, wie es in 10, 20 oder 30 Jahren sein wird. Es ist also sehr wichtig, dass Sie die richtige Behandlung erhalten. Und es ist eine sehr gute Sache, dass mehr Menschen von diesen billigeren Medikamenten profitieren können", sagt Connie Ziegler.